Volver a ¨Psicofarmacología – Psicodinámica IV (Indice General)¨
A) Clasificación Clínica
3-6. 1) Neurolépticos típicos o convencionales
La «convención» de llamarlos neurolépticos se debió a que fueron los primeros fármacos que aparecieron con acciones psiquiátricas (alucinolíticas) y neurológicas (sedación sin anestesia, extrapiramidalismos y acciones neurovegetativas).
a) Neurolépticos sedativos
Este grupo corresponde fundamentalmente a los derivados fenotiazínicos con cadena lateral alifática:
– Clorpromazina
– Clorprotixeno
– Clozapina (atípico)
– Levomepromazina
– Prometazina
– Properciazina
– Propiomazina
Poseen una acción hipnoinductora inicial y sus efectos colaterales son primariamente trastornos neurovegetativos (sudoración, taquicardia, hipotensión arterial) y, secundariamente, fenómenos extrapiramidales del tipo hipotónico-hiperquinético.
La acción antipsicótica (antidelirante-alucinolítica) comienza luego de un período de tratamiento, en general algo más prolongado que para los de tipo incisivo. Potencian a los analgésicos e hipnóticos y existen derivados químicos que se emplean como analgésicos.
En dosis bajas es común su uso en clínica médica, ya que se aprovechan sus efectos ansiolíticos, antieméticos y antialérgicos. También se los suele indicar en enfermedades psicosomáticas como la anorexia nerviosa, la colitis ulcerosa, la alergia inespecífica, etc. En este tipo de afecciones, donde la psicoterapia desempeña un rol prioritario, la «sensibilidad» del paciente puede ser mayor, presentándose síntomas o efectos colaterales tempranos (mareos, hipotensión ortostática, aumento de peso, etc.).
b) Neurolépticos incisivos
Este grupo comprende tanto derivados fenotiazínicos con cadena lateral piperazínica corno derivados de las butirofenonas y algunos grupos de síntesis reciente:
– Benperidol
– Benzamidas:
Amilsuprida
Sulpirida
Sultoprida
– Butilpiperazina
– Bromperidol
– Dixirazina
– Fluanizona
– Flufenazina
– Flupentixol
– Fluspirileno
– Haloperidol
– Lemperona
– Oxalflumazina
– Penfluridol
– Pimozida
– Pipotiazina
– Proclorperazina
-Tioproperazina
-Trifluoperazina
-Trifluoperidol
La denominación de este grupo de «antipsicóticos» específicamente proviene de sus acción rápida para yugular procesos delirantes y alucinatorios.
Se los puede asociar a los neurolépticos sedativos no solamente para balancear los efectos extrapiramidales sino como complementeo de sedación nocturna y aún diurna.
Las trifluoperazina y el haloperidol son los psicofármacos más conocidos de este grupo. Indiscutiblemente, desde su aparición hace más de 20 años, el haloperidol constituye el punto de referencia obligado para determinar la eficacia de los nuevos preparados.
El bromperidol es una nueva butirofenona que difiere del haloperidol en que posee una vida media más larga (15-35 horas), puede administrarse en una toma diaria, actúa rápidamente por vía oral y tiene afinidad por los receptores DA2 y 5-HT.
En un estudio comparativo con haloperidol, en 164 pacientes, la incidencia de efectos extrapiramidales (distonía aguda y acatisia) fue menor con bromperidol, y similar la incidencia de parkinsonismo. Las dosis usuales oscilan entre 3 y 20 mg/día.
El Trifluoperidol es más potente que el haloperidol, pero sus efectos neurológicos son más frecuentes e intensos que los de este último.
La pimozida es menos potente que los anteriores, pero sus efectos secundarios son menores y, por sus características farmacocinéticas (vida media de alrededor de 18 horas), puede administrarse en una única dosis diaria.
Los derivados difenilbutilpiperidínicos, que se caracterizan por su acción más prolongada: son el penfluridol y el fluspirileno. Si bien sus efectos secundarios son similares a los de los demás neurolépticos, la duración de su acción terapéutica los hace útiles para determinado tipo de pacientes.
El penfluridol se administra por vía oral y el fluspirileno por vía intramuscular, ambos una vez por semana. La duración prolongada del fluspirileno se debe a la micronización de la suspensión, que permite una lenta absorción desde el sitio de inyección.
El efecto retard del enantato de flufenazina y del palmitato de pipotiazina se debe a que forman una unión éster en el sitio de la inyección, lo cual permite una liberación gradual del principio activo de la droga, que se prolonga por espacio de dos semanas en el primer caso y de cuatro semanas en el segundo.
Las benzamidas sustituidas tienen tina acción bipolar caracterizada por Una acción desinhibidora en dosis bajas, y otra sedante en dosis altas, que se deberían a una afinidad diferente frente a los receptores dopaminérgicos.
Todos estos compuestos se caracterizan por su alta afinidad para los receptores DA2 y su baja ligadura con los de tipo alfa-adrenérgico, 5-HT2, HI y colinérgicos.
Los efectos adversos más comunes son temblor, disquinesia, ansiedad, trastornos del sueño, astenia, hipotensión y síndrome de galactorrea-amenorrea.
La sulpirida en dosis de 600 mg/d ha demostrado poseer un buen efecto desinhibidor. Aumentando la dosis a 1200 mg/d se obtiene una disminución de las ideas delirantes y alucinaciones, pero su acción en este sentido es menos eficaz que la de las butirofenonas.
En dosis bajas (50-200 mg/d) se la emplea en clínica médica por sus efectos antidepresivos (estimulantes). Los buenos efectos terapéuticos demostrados en pacientes con trastornos gastroentéricos (úlcera, gastritis, etc.) han sido ampliamente divulgados por la escuela francesa. Aún queda por dilucidar si estos efectos son primariamente producidos por el fármaco (efecto alfa-bloqueante) o, secundariamente, por su acción psicoestimulante y antiemética.
La amisulprida en dosis de 50 a 250 mg se la emplea para contrarrestar síntomas negativos, y entre los 400-800 mg/día, para el tratamiento de pacientes con síntomas positivos.
La remoxiprida es de rápida absorción, casi completa. Bloquea el DA2 pero con menos efectividad en la región nigroestriada, poca afinidad por el DA1 y escasa acción sobre receptores serotoninérgicos, histaminérgicos, muscarínicos y alfa-adrenérgicos y bajos efectos extrapiramidales. Su uso se ha discontinuado debido a discrasias sanguíneas.
La sultoprida (Barnetil, Francia) es inhibitoria en dosis de hasta 600 mg/ día y alucinolítica y antidelirante en dosis superiores a 1200 mg/día.
En clínica médica se la emplea, en dosis bajas, por sus efectos estimulantes. Su efecto colateral de excitación puede llegar a empeorar el cuadro psicótico.
c) Neuroléplicos de transición
Este grupo se caracteriza por compartir los efectos sedativos y antipsicóticos de los grupos anteriores. Esta característica los hace menos incisivos, pero son útiles en enfermos con impulsividad, agresividad, trastornos del carácter y procesos esquizofrénicos crónicos, en quienes se busca la «resocialización».
Comprende derivados fenotiazínicos con cadena lateral piperidínica y algunos otros de síntesis más reciente.
– Clotiapina
– Loxapina
– Tioridazina
En general estos neurolépticos presentan menores efectos anticolinérgicos y extrapiramidales, comparados con los demás grupos.
Sin embargo, pueden producir hipotensión ortostática, taquicardia y mareos al comienzo del tratamiento.
La tioridazina se usa habitualmente en geriatría, dada su menor incidencia de efectos extrapiramidales. Se han descrito trastornos de la eyaculación por su uso prolongado, motivo por el cual algunos autores la recomiendan como tratamiento en la eyaculación precoz. Este efecto se debería a la acción simpaticolítica a nivel de los plexos pélvicos, que bloquearía la eyaculación, en tanto que el efecto anticolinérgico provocaría la relajación del músculo detrusor de la vejiga, originando así una eyaculación retrógrada.
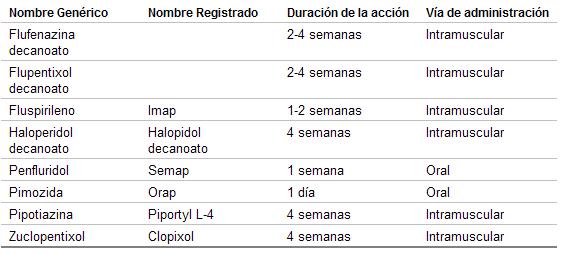
d) Neurolépticos de acción prolongada
Desde esta perspectiva, los neurolépticos se pueden dividir en dos categorías: de acción corta (o habitual) y de acción prolongada.
Los de acción corta son todos aquellos antipsicóticos cuya vida media (tiempo necesario para que la concentración inicial del psicofármaco se reduzca a la mitad) es de 4-8 horas, lo que permite que administrándolos cada 6-8 horas se mantenga una concentración plasmática, adecuada.
Los de acción prolongada permiten mantener concentraciones sanguíneas útiles por períodos que pueden llegar hasta las cuatro semanas.
Esta acción puede deberse a que el compuesto está micronizado (fluspirileno) o a que se mantiene en forma de depósito en el tejido muscular (pipotiazina, haloperidol decanoato).
Los psicofármacos de acción prolongada están especialmente indicados en los tratamientos que se caracterizan por:
1) La negativa que opone el enfermo a la administración de psicofármacos. Este tipo de resistencia no debe analizarse de forma aislada. Se debe tener en cuenta no sólo el negativismo del paciente sino el de los familiares responsables, quienes suelen utilizar al enfermo como «depósito» de la psicosis familiar y no desean el cambio en los roles que puede ocasionar la medicación.
2) El peligro de que el paciente intente suicidarse cuando se le indica medicación a largo plazo.
3) La negativa a tomar medicación psicofarmacológica por la crítica social (real o fantaseada) cuando el paciente desarrolla sus tareas laborales habituales.
4) La no aceptación de la enfermedad y, por consiguiente, de la medicación.
5) La necesidad de que la «institución», al no haber familiares responsables o continentes del enfermo, se haga cargo de la administración psicofarmacológica.
6) La necesidad de evitar la variabilidad en la absorción gastrointestinal y en la concentración plasmática, frente a absorciones erráticas naturales o provocadas por la mala compliance del paciente (no tomar la medicación de acuerdo con la directiva médica en lo que se refiere a dosis y horarios).
Si bien estas formas farmacéuticas permiten obtener concentraciones plasmáticas útiles, poseen el inconveniente de que, si presentan efectos secundarios, éstos deberán ser yugulados con otras drogas, ya que una vez administradas no será posible impedir la lenta liberación del neuroléptico activo, almacenado en el tejido muscular.
Antipsicóticos de depósito o de acción prolongada
Los efectos secundarios que producen son los habituales para todos los neurolépticos. Su aparición puede ser muy precoz, en especial síntomas depresivos o desinhibitorios.
En estos casos, es importante prestar especial atención al relato del paciente. Se deberán extremar los cuidados ante las fantasías de suicidio u homicidio y los sueños directa o indirectamente vinculados a la muerte.
De los efectos adversos extrapiramidales la disquinesia tardía y la acatisia y aquinesia con trastornos disfóricos son los más importantes.
La disquinesia tardía clásicamente descrita ya no constituye una enfermedad irreversible o mortal, pues se pudieron establecer con mayor precisión las poblaciones de riesgo y adecuar el tratamiento.
Las poblaciones de riesgo a las que se debe prestar particular atención son las mujeres en la tercera edad, enfermos con antecedentes extrapiramidales y con enfermedad de Huntington o Wilson, y los pacientes que presentan trastornos afectivos asociados.
Los síntomas de disquinesia tardíos que pueden aparecer durante la administración de neurolépticos de depósito deberán evaluarse de acuerdo con la ecuación de beneficios/ molestias que ocasiona este tipo de medicación. Los chasquidos de lengua, las muecas en la expresión facial, los movimientos de dedos, miembros o del tronco, pueden llegar a provocar, más que molestias de orden estético o ambiental, dificultades para hablar, comer o caminar.
Con respecto a los síntomas depresivos o aquinético-depresivos, deberán ser tenidos en cuenta en función de que el paciente crónico presenta habitualmente episodios depresivos durante el transcurso del proceso esquizofrénico.
La pimozida y el penfluridol deben su efecto prolongado a sus características farmacocinéticas específicas. El fluspirileno posee un efecto retard porque se encuentra micronizado en suspensión acuosa. La flufenazina, la pipotiazina y el decanoato de haloperidol se presentan como una combinación de tipo ácido graso-éster que libera el compuesto activo de forma gradual desde el sitio de inyección.
La ventaja que tendría el fluspirileno sobre la flufenazina y la pipotiazina es no producir abscesos, por tratarse de una suspensión acuosa. Sin embargo, deberán controlarse periódicamente los diferentes sitios de inyección, pues algunos enfermos, luego de prolongadas administraciones, presentan necrosis aséptica del tejido conectivo, debido a la absorción rápida del vehículo acuoso y a la precipitación de los cristales de fluspirileno, que puede producir efectos tóxicos locales.
La oxaflumazina actúa en dosis bajas (20-50 mg/d) como desinhibidor, y en dosis altas (300-600 mg/d) como sedante.
El zuclopentixol en dosis altas es usado por sus efectos estimulantes; en dosis menores presenta actividad ansiolítica y antidepresiva.
La equivalencia entre el decanoato de haloperidol y haloperidol oral debe ajustarse, según el enfermo, entre 10-20 mg/d por vía intramuscular por cada mg administrado por vía oral.
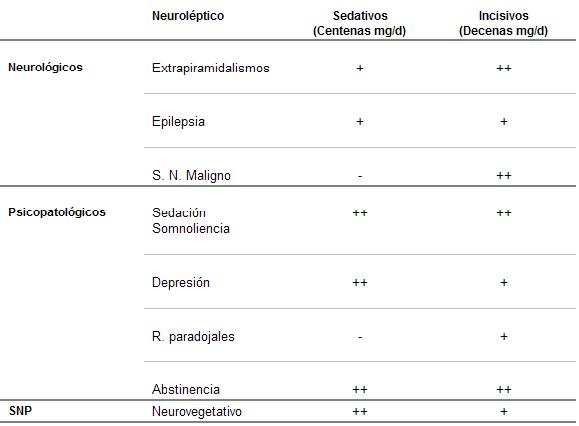
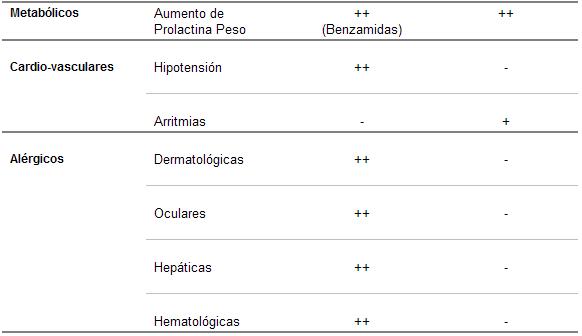
Efectos adversos de los antipsicóticos típicos o convencionales
Los neurolépticos producen efectos secundarios en un porcentaje de casos que varía desde 0 hasta 90 por ciento, de acuerdo con diferentes estadísticas.
Esta disparidad se debe a que se engloban dentro de los efectos adversos ciertos efectos propios de la medicación (como los anticolinérgicos o extrapiramidales) y los efectos alérgicos y tóxicos.
Cuadro 20. Efectos adversos de los neurolépticos típicos o convencionales
Estas diferencias pueden atribuirse a la hipersensibilidad de los receptores dopaminérgicos en las estructuras mesolímbicas. Esta concepción estaría avalada clínicamente por la necesidad de aumentar la dosis en los tratamientos crónicos (¿tolerancia?) y por la aparición de un síndrome de abstinencia cuando se suspende bruscamente el antipsicótico (¿dependencia?).
Por estos motivos, no se deberían usar los neurolépticos durante lapsos muy prolongados, salvo en aquellos enfermos sobre quienes su eficacia clínica pueda ser demostrada. Es conocido el hecho, aún sin comprobación estadística, de que las medidas de contención psicoterapéuticas (psicoterapias, hospital de día, terapias múltiples, etc.) disminuyen notablemente la necesidad de la administración de dosificaciones altas y prolongadas.
A) Acciones adversas neurológicas
1) Síndromes extrapiramidales
Etiología y factores que inciden en su aparición. Pueden presentarse durante el tratamiento con neurolépticos (síndrome extrapiramidal de tipo precoz), luego de un tratamiento prolongado o después de interrumpir la medicación neuroléptica (síndromes extrapiramidales de tipo tardío).
Los distintos autores dan diferentes frecuencias de aparición que oscilan entre el 0 y el 66 % en las disquinesias precoces y entre el 0 y el 8 % en las disquinesias tardías.
Para una función motora equilibrada, es necesario que el sistema extrapiramidal (tracto nigroestriado) posea un balance adecuado entre las acciones dopaminérgicas (inhibitorias) y las colinérgicas (excitatorias). Un balance con predominio colinérgico originará síndromes extrapiramidales de tipo precoz, en tanto que un balance con predominio dopamínico provocará disquinesias tardías.
Los neurolépticos, al bloquear los receptores dopaminérgicos, ocasionan síntomas similares a los de la enfermedad de Parkinson. Los anticolinérgicos disminuyen la predominancia colinérgica del sistema nigroestriado, restableciendo así el balance dopamina-acetilcolina.
En la enfermedad de Parkinson existe un déficit real de dopamina por lesiones atróficas de las células dopaminérgicas del sistema nigroestriado.
En general, las disquinesias aparecen al comienzo del tratamiento con neurolépticos, en tanto que los restantes síndromes se manifiestan luego de las tres semanas de haberlo comenzado.
En realidad, el desarrollo de un síndrome extrapiramidal medicamentoso puede preverse si se tienen en cuenta ciertos antecedentes del paciente:
Sexo. Las mujeres poseen niveles más elevados de MAO que los hombres, lo que provoca un aumento de la degradación de dopamina. Los niveles de estrógeno influyen en el metabolismo de las catecolaminas. Se deben tener en cuenta el embarazo y parto. En los hombres de edad avanzada, los bajos niveles de testosterona circulante provocan una inhibición de la degradación de las catecolaminas.
Edad. En general se puede afirmar que las disquinesias se presentan antes de los 40 años, la acatisia en la edad mediana y los síndromes parkinsonianos en la tercera edad.
Estas diferencias en la susceptibilidad a las afecciones citadas tienen un correlato bioquímico: al avanzar la edad aumenta la MAO y disminuye la dopa-decarboxilasa, lo que provoca un incremento en la destrucción de dopamina (por la MAO) y una inhibición de su producción (por la dopadecarboxilasa).
Factores genéticos. Familias con antecedentes de enfermedad de Parkinson idiopática tenderán a presentar una alta incidencia de extrapiramidalismo de origen medicamentoso. De allí la importancia de investigar cuidadosamente los antecedentes familiares del paciente, antes de comenzar a administrar la medicación neuroléptica.
Diferencias individuales de biodisponibilidad. Las variaciones individuales de absorción, metabolismo y susceptibilidad incidirán en la aparición de los distintos síntomas extrapiramidales.
Características del neuroléptico prescrito. El efecto extrapiramidal del neuroléptico está vinculado a su menor efecto anticolinérgico y al sitio de acción del bloqueo dopamínico.
Así, por ejemplo, la clozapina y la tioridazina son las que poseen mayor efecto anticolinérgico y menores efectos extrapiramidales en comparación con el haloperidol o la trifluoperazina.
Estas diferencias se deben a que los psicofármacos mencionados bloquean sistemas celulares dopaminérgicos de distintos núcleos del sistema nervioso central: el haloperidol, por ejemplo, bloquea los núcleos de la sustancia nigra y la clopazina los del sistema límbico.
Dosis, tiempo de administración e interacciones. hasta hace poco se creía que la dosificación alta incrementaba la incidencia de síntomas extrapiramidales. En realidad, la acción anticolinérgica que producen los neurolépticos logra finalmente disinuir esos síntomas.
El tiempo prolongado de adinistración de antipsicóticos incide en la aparición de los síndromes extrapiramidales de tipo tardío.
La interrupción brusca luego de un tiempo prolongado de administración, la continuación posterior luego de una interrupción, aun con neurolépticos de otros grupos farmacológicos, son factores altamente potenciadores del desencadenamiento de esos síndromes.
Los agentes antitiroideos, los corticoides, los inhibidores del calcio v el hipertiroidismo pueden desencadenar síndromes extrapiramidales.
a) Síndromes extrapiramidales precoces
Disquinesias o distonías agudas (fenómenos excitomotores).
Se presentan como contracciones tónicas involuntarias de músculos estriados (crisis oculógiras, tortícolis, lordosis, espasmos de lengua y boca, cte.). Es la manifestación más precoz, se observa entre la primera hora y los dos días subsiguientes. Aparece en el 2,5 – 5 % de los pacientes, no es necesariamente dosis dependiente y, afecta más a niños y adultos jóvenes.
Conviene señalar que este tipo de fenómenos excitomotores pueden manifestarse en cualquier parte del organismo, aun con síntomas muy vagos. Pueden ser confundidos con reacciones histéricas, meningitis, encefalitis, epilepsia, etcétera. En general la sintomatología desaparece en pocos minutos.
Algunos medicamentos como la metoclorpropamida, usada como antiemético, el antihistamínico difenilhidramina y la anfetamina pueden producir disquinesias agudas.
Se puede: disminuir la dosis del neuroléptico, utilizar antiparkinsonianos por vía IM o IV o agregar benzodiazepinas.
Acatisia.
Es tina agitación motriz acompañada generalmente de ansiedad y/o angustia. El enfermo no puede quedarse quieto, camina constantemente. Cuando se sienta no cesa de mover sus piernas.
Aparece en el 20 %, al cabo de días, meses, o años. Los antipsicóticos incisivos y de acción prolongada lo inducen más frecuentemente, y menos el litio, los antidepresivos tricíclicos y la fluoxetina.
El insomnio y la angustia por lo común inducen a pensar en una dosificación insuficiente del neuroléptico y, por lo tanto, a aumentar la dosis. En ocasiones la angustia que acompaña a la forma precoz (no a la tardía), puede inducir al suicidio. Es conveniente observar con mucha atención al paciente, sentado y parado.
Aquinesia.
Se caracteriza por debilidad, fatiga, abulia, apatía, repetición de movimientos, hipomimia (mirada de zombie), cte. Puede haber también dolores musculares y articulares.
Deberá realizarse el diagnóstico diferencial entre el efecto sedante provocado por los neurolépticos, con los síntomas de tina depresión y, con la enfermedad esquizofrénica de tipo catatónico.
Síndrome parkinsonoide.
La rigidez, la aquinesia y el temblor constituyen los síntomas más comunes. Este síndrome se presenta, en un alto porcentaje de casos, precedido por acatisia, aquinesia y sequedad de boca o hipersalivación. La rigidez es hipertónica y no espástica (signo de la rueda dentada), y comienza en forma proximal para hacerse luego distal.
Es la manifestación más frecuente, 40 % – 90 %, más común en pacientes ancianos.
La sialorrea,
la intolerancia al calor, la seborrea y cualquier otro signo o síntoma de la enfermedad de Parkinson se pueden presentar de forma aislada o juntamente con otros.
El temblor
puede presentarse cuando el enfermo ejecuta movimientos o cuando descansa. Por lo común aparece en los dedos de la mano, pero puede generalizarse a la boca, lengua, etc. («síndrome del conejo»). Se diferencia del temblor producido por el litio o los antidepresivos tricíclicos en que su frecuencia es más lenta y en que responde al tratamiento con fármacos antiparkinsonianos.
b) Síndromes extrapiramidales tardíos (disquinesia tardía)
La disquinesia tardía es un síndrome caracterizado por movimientos involuntarios faciobucales, coreicos y atetósicos, y por tics. Los más comunes son los movimientos de la lengua, el inflamiento de los carrillos, el chupeteo de los labios. Se puede agregar además un síndrome de tipo parkinsonoide. Los movimientos empeoran con las reacciones emocionales y disminuyen con la sedación.
Hasta hace pocos años se consideraba que este síndrome aparecía en la tercera edad, de seis a doce meses después de la suspensión de un tratamiento prolongado con neurolépticos y acompañado de daño cerebral. Es más común cuando se han usado grandes dosis y durante largo tiempo.
En la actualidad, las disquinesias tardías se han puesto más de manifiesto debido a que a los enfermos mentales no se los trata ya con psicofármacos «de por vida».
El tratamiento intermitente, la reiniciación de la medicación en los períodos agudos, si bien es beneficioso, ha hecho más notoria la aparición de la disquinesia tardía en un porcentaje de enfermos.
Se observa en el 20 % de los pacientes, de los cuales en un 8 % puede ser severa y en un 1 % irreversible.
c) Tratamiento de los síndromes extrapiramidales
Al igual que los tratamientos psicofarmacológicos habituales, el de los efectos colaterales despierta en el enfermo y en el médico diferentes expectativas.
La sensación de fracaso, desamparo y aun de muerte provocada por el efecto colateral en el enfermo aumentará su sensación de abandono si el profesional interviniente no demuestra conocer lo que le sucede y no se hace reconocer como idóneo, adoptando medidas terapéuticas que lo alivien.
Será necesario, al igual que con cualquier medicación psicofarmacológica, elaborar un plan de acción que debe ser comunicado al enfermo, al familiar responsable y al psicoterapeuta. Dicho plan abarcará no solamente la medicación contra el efecto colateral, sino las demás medidas de contención. Estas comprenden la tranquilización del medio y la ayuda al personal auxiliar para que no se sientan molestos por las recriminaciones del enfermo.
Tratamiento de los síndromes extrapiramidales precoces
Las estadísticas sobre la eficacia de la administración de antiparkinsonianos con finalidad profiláctica en el curso del tratamiento con neurolépticos son aún contradictorias (ver también cap. 19, 19-7).
El tratamiento a largo plazo puede no ser necesario para algunos pacientes.
Por otra parte, los antiparkinsonianos pueden disminuir los niveles sanguíneos de neurolépticos y aumentar el riesgo de que sobrevengan disquinesias tardías o síndromes anticolinérgicos agudos. Es recomendable que antes de decidir sobre el empleo profiláctico de antiparkinsonianos se tengan en cuenta la historia familiar del enfermo y los puntos más arriba enumerados.
Cuadro 21. Ventajas y desventajas de los antiparkinsonianos
– No hay demostración cabal de profilaxis.
– No todos los pacientes desarrollan extrapiramidalismos.
– Aumentan el riesgo de que se produzcan disquinesias tardías.
– Pueden disminuir los niveles plasmáticos de neurolépticos.
– Pueden causar, citando se administran juntamente con neurolépticos y/o antidepresivos, síndromes anticolinérgicos.
– Se deben indicar en pacientes con antecedentes personales o familiares de extrapiramidalismos.
De presentarse un síndrome extrapiramidal se deberá intentar:
1) Una reducción de la dosificación neuroléptica.
2) Utilizar anticolinérgicos en dosis crecientes.
3) Agregar benzodiazepinas (diazepam) o agonistas dopaminérgicos (amantadina).
4) Si estos últimos fracasan, se impone la sustitución del neuroléptico utilizado por otro que pertenezca a un grupo diferente.
En la acatisia es pobre el efecto que se logra con anticolinérgicos o benzodiazepinas. Dado que se la atribuye a un bloqueo dopaminérgico en estructuras no estriadas; se puede intentar el empleo de beta-bloqueantes (propranolol) o de clonidina.
En caso de suspenderse la medicación anticolinérgica, ésta deberá realizarse de forma lenta y gradual y se continuará aun después de no administrarse más el antipsicótico, a fin de evitar fenómenos extrapiramidales rebote.
La supresión del agente anticolinérgico, puede provocar la emergencia de la bradiquinesia y a veces su empeoramiento en alrededor del 68 % de los pacientes.
Los anticolinérgicos per se también pueden provocar trastornos de las funciones mnésicas y cognitivas. Pueden ser adictivos cuando se los combina con neurolépticos de baja potencia (clozapina, clorpromazina, tioridazina), muchos de los cuales tienen sus propios efectos anticolinérgicos.
La amantadina, carece de efectos anticolinérgicos y puede ser tina alternativa eficaz en el tratamiento del síntomas extrapiramidales precoces.
Anticolinérgicos naturales:
Atropina
Anticolinérgicos sintéticos:
Biperideno
Cicrimina
Dexetimida
Orfenadrina
Prociclidina
Trihexifenidilo
Todos los antiparkinsonianos producen efectos terapéuticos similares; en relación con uno de ellos, el trihexifenidilo, se han descrito casos de adicción. El biperideno se presenta en tabletas, cápsulas retard y ampollas. Administrado por vía intravenosa, comienza a producir efecto a los pocos minutos, con un pico máximo a las 4 horas. Con las tabletas en las dosis habituales (34 mg/día), el comienzo de acción se presenta alrededor de las 24 horas.
La forma retard se prescribirá cuando convenga espaciar las dosis; es necesario en tal caso evaluar la función hepática del paciente (por la absorción diferida) y su sensibilidad alérgica (por las características del retard).
Los anticolinérgicos de este tipo presentan sus propios efectos colaterales (síntomas neurovegetativos, efecto paradójico). Pueden potenciarse con neurolépticos y/o antidepresivos y dar origen a cuadros de tipo tóxico (inquietud, confusión anticolinérgica, reacciones psicóticas).
Tratamiento de los síndromes extrapiramidales tardíos
(disquinesia tardía).
Es conveniente esperar unos días antes de restituir el tratamiento neuroléptico, en especial si la disquinesia es bien tolerada, ya que, según se ha podido comprobar, en algunos casos desaparece espontáneamente de forma lenta y gradual. El empleo de antiparkinsonianos es contraproducente. En caso de empeoramiento, el tratamiento es difícil y aún no existe una droga de elección.
En general conviene retirar el antipsicótico y cambiar por un atípico.
La mejor profilaxis es usar dosis y tiempos mínimos efectivos y después de tres meses de iniciado el tratamiento, si es posible, retirar el antiparkinsoniano.
Además del cambio del neuroléptico se puede intentar el uso de agentes colinérgicos (fisostigmina, colina), se producen mejorías en un 25 %, pero habitualmente son transitorias.
También se han usado compuestos gabaérgicos (valproato, benzodiazepinas: clonazepam), amantadina y L-dopa. Menos satisfactorios han sido los tratamientos con reserpina, propranolol y clonidina.
Más recientemente se han usado en el tratamiento de la disquinesia tardía, bloqueantes cálcicos como el verapamil, nifedipina y diltiazem con buenos resultados. El calcio estaría implicado en la síntesis y la liberación de dopamina; sus antagonistas inhibirían estos mecanismos.
El efecto se debería entonces a una reducción de la actividad dopaminérgica en el nigroestriado (alta densidad de receptores a los antagonistas cálcicos se han encontrado en la sustancia nigra).
Sin embargo la clozapina es en la actualidad, por su selectividad mesolímbica, una de las drogas usadas con mayor éxito.
2) Epilepsia
Los antipsicóticos sedativos o de baja potencialidad (dosificables en cientos de mg) producen una disminución del umbral convulsivo.
Esta acción epileptógena puede aparecer en pacientes considerados hasta ese momento como no epilépticos, y aun cuando se utilicen dosis medianas o altas durante lapsos breves.
En enfermos con antecedentes epilépticos es recomendable administrar dosis bajas de neurolépticos sedantes. Otras alternativas son cambiar a una estructura química más incisiva, aumentar las dosis de los antiepilépticos que el paciente tomaba con anterioridad o incluir estos últimos como medicación preventiva.
Se deberá prestar atención a los antecedentes que incluyan el uso de drogas adictivas o alcohol, ya que en estos casos la vulnerabilidad epileptógena es mayor.
3) Síndrome neuroléptico maligno
Es una complicación grave del tratamiento neuroléptico, probablemente de naturaleza idiosincrásica. Se presenta generalmente en los inicios (3-9 días) del tratamiento con neurolépticos, aunque se han descrito casos de aparición en cualquier momento de su transcurso.
Es más común en hombres jóvenes (1,5 más que en mujeres) y en pacientes con trastornos afectivos, daño cerebral orgánico y alcoholismo. Su incidencia es de 0,5-1,4 %.
Aunque todos los antipsicóticos pueden ocasionarlo, aparece más frecuentemente asociado a los del grupo de alta potencia (dosificables en décimos de mg), los de acción prolongada y los que se administran por vía intravenosa.
El mecanismo permanece desconocido. Se lo involucra en una patología similar a la del síndrome hipertérmico maligno de origen anestésico con lesiones en las estructuras hipotalámicas y en los ganglios de la base, donde existiría una falla en la regulación de los mecanismos dopaminérgicos que controlan el tono muscular y autónomo, por bloqueo del receptor dopamínico. Las complicaciones más graves son rabdomiólisis con mioglobinuria, insuficiencia renal, coagulación intravascular, tromboembolismo pulmonar e insuficiencia respiratoria.
Un 20 % de los casos presenta un desenlace mortal.
El cuadro clínico, que se instala entre 24-72 horas, es el siguiente:
1 ) Temperatura muy elevada.
2) Síndrome neurológico: alteraciones de la conciencia, mutismo, aquinesia, extrapiramidalismos, rigidez muscular.
3) Síndrome neurovegetativo: taquicardia, hipertensión, hiperpnea, sudoración, deshidratación.
4) Síndrome bioquímico: leucocitosis, aumento de la creatinfosfoquinasa plasmática.
Las medidas terapéuticas deben incluir la suspensión del neuroléptico de manera inmediata, medidas sintomáticas (enfriamiento, hidratación) y utilización de agonistas dopaminérgicos como la bromcriptina en dosis de 15-80 mg/día o la amantadina de 200-400 mg/día.
En casos de contracciones se aconseja el uso de dantrolene que facilita la reabsorción de calcio desde el mioplasma al sarcoplasma para restablecer la relajación muscular, ya que actúa periféricamente. Las dosis oscilan entre 14 mg/kg/día por vía intravenosa, para continuar luego por vía oral (25-330 mg/d). También se ha intentado el tratamiento con bloqueantes de calcio que desplazan la ligadura del neuroléptico del receptor D2 o disminuyen el calcio intracelular, y con benzodiazepinas por vía intravenosa. Deberán evaluarse los efectos adversos que produce cada tratamiento; así por ejemplo, los agonistas dopaminérgicos pueden acentuar la psicosis, y el dantrolene es hepatotóxico.
Los anticolinérgicos pueden empeorar el cuadro al aumentar la hipertermia y disminuir la sudoración. La hipotensión, producto de la vasodilatación y el bloqueo alfa-adrenérgico, puede corregirse con noradrenalina y la sobreactividad simpaticomimética con beta-bloqueantes.
Es conveniente prestar atención a las medidas de contención familiar, explicando la gravedad del cuadro y la posibilidad de un desenlace fatal.
B) Acciones adversas psicopatológicas
1) Sedación con somnolencia
Como ya se mencionó con anterioridad, para demostrar la efectividad de un tratamiento antipsicótico no es necesaria la aparición de fenómenos extrapiramidales, ni tampoco de la sedación. Obviamente, estos efectos son más comunes en el grupo de neurolépticos sedativos. Generalmente se produce tolerancia al cabo de tinas semanas. Si la sedación o somnolencia diurna resultan molestas, se puede indicar el antipsicótico en una toma diaria antes de acostarse.
2) Depresión
3) Reacciones paradojales con excitación
C) Acciones adversas neurovegetativas
Se denomina «sistema autónomo» a las neuronas y fibras eferentes por intermedio de las cuales llegan los impulsos nerviosos a los tejidos y órganos periféricos que no sean los músculos estriados o esqueléticos. En sentido estricto, representarían solamente la porción motriz periférica de la inervación visceral. Sin embargo, últimamente se llama «autónomo» al sistema neurovegetativo que incluye:
– El sistema aferente, que recoge la información visceroceptiva, cuyos cuerpos neuronales se alojan en los ganglios cerebroespinales.
– Los centros cerebrales superiores que regulan todo el sistema autónomo desde la corteza.
– El sistema eferente propiamente dicho con su primera neurona preganglionar (cuyo neurotransmisor es la acetilcolina) y su segunda neurona posganglionar (cuyo mediador químico es la adrenalina en el sistema simpático y la acetilcolina en el sistema parasimpático).
En general, la neurona posganglionar del sistema simpático se localiza en los ganglios espinales, en tanto que la del sistema parasimpático se encuentra en el órgano efector terminal.
Si bien los impulsos corticales neurovegetativos son involuntarios y permanecen en un nivel inconsciente, existe un determinado «tono de bienestar visceral neurovegetativo» de base en el cual se mezclan sensaciones afectivas y propioceptivas (profundas, difusas o circunscriptas) de acuerdo con los estímulos aferentes de los distintos órganos (dolor visceral, hambre, taquicardia, etc.).
La mayoría de los órganos torácicos (corazón, pulmón) y abdominales (intestino, hígado) tienen inervación parasimpática cuya neurona preganglionar se halla en el nervio craneal vago (l0′ par) y sus neuronas posganglionares en el efector terminal.
Más que la comprensión de las relaciones estructurales del sistema neurovegetativo, importa analizar aquí la regulación neuroquímica, aún hoy de difícil estudio.
Originalmente, las especies animales primitivas tienen un sistema binario para interactuar con el medio: el trofotrópico (anabólico o parasimpático cuyos mediadores son la serotonina y la acetilcolina) y el ergotrópico (catabólico o simpático mediado por la noradrenalina y la dopamina).
Con el desarrollo evolutivo, este tipo de respuestas pasaron a ser autónomas en la especie hasta llegar a los primates y seres humanos, donde un nuevo sistema dopaminérgico permite retardar o acelerar la respuesta, y así captar la percepción, el aprendizaje y la memoria del mundo exterior.
La adrenalina ya no tiene acceso al sistema nervioso central, al no atravesar la barrera hematoencefálica, en tanto que las células productoras de dopamina, a diferencia de las de la noradrenalina, maduran tardíamente después del nacimiento. De esta manera, la clásica respuesta binaria (huida-enfrentamiento; contracción-dilatación de los vasos sanguíneos; estimulación-inhibición de las glándulas de secreción), representada por el sistema autónomo periférico adrenérgico (simpático) o colinérgico (parasimpático), se transforma en una respuesta mucho más compleja ya no binaria al poder ser valorada por un «sistema autónomo central» donde, por intermedio de neuronas y mediadores neuroquímicos, el individuo puede establecer un nuevo control sobre el mundo exterior y sobre su propio mundo interno, frente a cada nuevo estímulo.
La noradrenalina y la serotonina son ahora reguladas por otro sistema que depende de la dopamina y acetilcolina. Este tipo de regulaciones permite retrasar o acelerar, luego de una valoración, qué tipo de respuesta será la más adecuada.
Dentro de ciertos límites, el sistema funciona en equilibrio con una resultante, producto de la sumatoria neuroquímica. Excedido, predominará un tipo específico de respuesta a través de un determinado neurotransmisor, tomando así el comando en el tipo de respuesta.
En los últimos años ha despertado mucho interés conocer qué tipo de respuestas periféricas desencadena el desequilibrio del sistema autónomo central. Así por ejemplo, la respuesta galvánica epidérmica puede variar al alterarse las resistencias por el aumento de la sudoración de la piel, que diferentes estados emotivos pueden provocar.
También el registro manométrico de la presión intracolónica reacciona sensiblemente a estos cambios de origen central ya que aquí también, como en la piel, el órgano efector colinérgico se encuentra en la parte terminal (plexo mientérico de Auerbach).
Los sistemas mesoestriados (núcleos putamen y amígdala) y el mesolímbico (tubérculos olfatorios) serían el lugar donde se entrecruzaría toda la información de origen autónomo antes de llegar a la corteza y otros núcleos.
Efectos periféricos
Antiadrenérgicos: congestión nasal, trastornos de la eyaculación, hipotensión postural (especialmente en gerontes).
Anticolinérgicos: El bloqueo del receptor muscarínico, que se encuentra en las neuronas posganglionares, ocasiona fenómenos similares al bloqueo de tipo atropínico.
La clozapina y la tioridazina son las que presentan mayor potencia anticolinérgica, en tanto los neurolépticos incisivos son los que determinan menores efectos.
Los gerontes son muy sensibles a estas acciones.
Los enfermos con glaucoma de ángulo abierto presentan pocos inconvenientes cuando se los compara con los de ángulo cerrado.
Las molestias que estos efectos causan son las siguientes:
Piel y mucosas: sequedad, enrojecimiento, calor.
Ojos: trastornos en la acomodación visual, aumento de la presión intraocular.
Aparato circulatorio: taquicardia, hipotensión.
Aparato gastrointestinal: disminución de las secreciones gástricas e intestinales, disminución de la motilidad y constipación.
Aparato urinario: menor contracción del músculo liso con retención urinaria. Puede tratarse con agonistas colinérgicos.
Aparato genital: disfunciones sexuales como
a) eyaculación retardada o retrógrada (se han usado distintos fármacos: neostigmina;
b) dificultades en la erección y
c) anorgasmia (a veces mejora, tratada con ciproheptadina (ver cap. 6, 6-18).
Luego de algunas semanas puede aparecer tolerancia a estos efectos periféricos, de lo contrario es conveniente contrarrestarlos con medicación apropiada o cambiar a neurolépticos incisivos.
Efectos centrales
El bloqueo de los receptores muscarínicos centrales produce trastornos en la memoria, síntomas confusionales y delirantes.
Las alteraciones mnésicas y confusionales son susceptibles de incrementarse notablemente en enfermos de la tercera edad que ya presentaban déficit cognoscitivos atribuibles a menores disponibilidades de acetilcolina central (predemencias, pseudodemencias, demencias metabólicas, etc.).
Síndrome anticolinérgico agudo
La asociación de neurolépticos sedantes con antiparkinsonianos y antidepresivos tricíclicos incrementa los riesgos tóxicos (centrales y periféricos) de los antipsicóticos.
La confusión, la agitación, la desorientación, las pupilas midriásicas, la piel seca y roja y la taquicardia denotan la gravedad tóxica anticolinérgica.
La terapéutica deberá realizarse con anticolinesterasas. Las anticolinesterasas terciarias (eserina) penetran en la célula nerviosa, se combinan rápidamente de forma inestable con la colinesterasa, evitando así la destrucción de la acetilcolina.
Se produce una buena oferta de acetilcolina en el receptor muscarínico y en la médula espinal donde actúa como estimulante. Por el contrario, las anticolinesterasas cuaternarias deprimen la médula espinal, son más estables en su combinación con las colinesterasas pero no penetran en la neurona, actuando por contacto en la membrana.
El aumento abrupto de la acetilcolina puede provocar bradicardias graves, reversibles con atropina.
Se deberá evaluar el tratamiento por vía intravenosa e intramuscular [eserina, neostigmina] u oral [neostigmina o piridostigmina].
D) Acciones adversas sobre el metabolismo y las glándulas endocrinas
En la mujer
El síndrome de galactorrea-amenorrea se debe a un bloqueo dopaminérgico a nivel hipotalámico que produce un aumento de la liberación de prolactina por la hipófisis anterior. Dejan de aparecer los picos normales de hormona luteinizante, estradiol y progesterona.
Estas alteraciones hormonales coinciden con una disminución de la libido sexual, generalmente ya disminuida en este tipo de pacientes.
No hay demostración de que el tratamiento crónico con neurolépticos pueda provocar cáncer de mama o adenomas hipofisarios lactotropos. Sin embargo, se deben controlar periódicamente las mamas y los niveles de prolactina plasmática. Valores superiores a los normales (545 ng/ml) pueden demostrar un bloqueo dopaminérgico hipotalámico efectivo. Cifras de 3 dígitos hacen sospechar la presencia de una hipertrofia o adenoma prolactínico que el especialista deberá evaluar.
La sulpirida es el neuroléptico de acción más intensa sobre este eje. Antes de usar bromocriptina (agonista dopaminérgico) se recomienda disminuir la dosis del antipsicótico o cambiar a otro de un grupo químico diferente.
En el hombre
La ginecomastia y los trastornos sexuales en el hombre coinciden con una elevación de los niveles plasmáticos de prolactina y con un descenso de los niveles de testosterona circulante.
Los pacientes describen una disminución de la libido sexual, una dificultad en mantener la erección y en las molestias de eyaculaciones retardadas o retrógradas. En este último caso hay orgasmos sin eyaculación, seguida luego de emisión de orina con características «espumosas».
Los antipsicóticos con fuerte acción anticolinérgica, en especial la tioridazina, son los que provocan estos fenómenos.
Aumento de peso
La administración crónica de neurolépticos produce aumento de peso corporal que se atribuye a la poca actividad corporal, al mayor sedentarismo y al incremento del apetito, probablemente de origen hipotalámico debido al efecto antihistamínico central.
La molindona y la loxapina tienen, por el contrario, un efecto anorexígeno cuyo origen se desconoce. Para controlar este efecto se recomienda lograr el equilibrio dietético, de la actividad corporal y de los ejercicios físicos lo más adecuado posible.
La clorpromazina altera la prueba de tolerancia a la glucosa y la liberación de insulina.
Las acciones sobre la glucemia y las hormonas tiroideas y de crecimiento no son relevantes. En algunos casos, puede registrarse el aumento de secreción antidiurética con polidipsia.
E) Acciones adversas cardiocirculatorias
Hipotensión arterial
La hipotensión arterial es más común durante la administración de neurolépticos de baja potencia (los dosificables en cientos de mg), en las formas parentales y con las fenotiazinas alifáticas (clorpromazina, levomepromazina).
Si bien es un efecto que puede producir tolerancia, se debe prestar atención a los enfermos con labilidad cardiovascular (hipotensos comunes o posturales) y a los gerontes.
La acción hipotensora es debida a una combinación de los efectos centrales hipotalámicos y periféricos de tipo bloqueante alfa-adrenérgico.
En casos de severa hipotensión se recomiendan las siguientes medidas:
1 ) Poner al paciente en posición decúbito horizontal.
2) Dar alimentos ricos en cloruro de sodio (jamón crudo, caldos concentrados, etc.).
3) Indicar expansores plasmáticos.
4) Utilizar estimulantes alfa-adrenérgicos puros (metaraminol, norepinefrina).
5) No usar estimulantes alfa y beta-adrenérgicos (tipo adrenalina) o beta-adrenérgicos puros (tipo isoproterenol), ya que la estimulación beta puede aumentar la hipotensión.
Arritmias
Los neurolépticos pueden ser antiarrítmicos o arritmógenos.
Este último efecto puede llegar a producir la muerte súbita por fibrilación ventricular, al prolongarse los períodos PR, QT y ST por aumento del período de repolarización y por efecto de tipo quinidínico tóxico directo sobre el miocardio.
El efecto antiarrítmico se debe a una acción simpática sobre el hipotálamo y a un efecto directo sobre la membrana celular al competir, igual que el anestésico lidocaína, con los lugares de fijación del calcio y al impedir la incorporación de fósforo a los fosfolípidos y el transporte activo de sodio y potasio.
En caso de intoxicación no deben usarse antiarrítmicos de tipo quinidínico como la procainamida, sino los similares a la lidocaína, la fenitoína, el propranolol o la fisostigmina.
En caso de arritmias tóxicas graves puede ser necesario recurrir a marcapasos. La tioridazina es particularmente cardiotóxica, potenciándose especialmente con la amitriptilina.
F) Acciones adversas alérgicas
Dermatológicas
Luego de uno a dos meses de tratamiento con antipsicóticos pueden aparecer reacciones maculopapulosas, dermatitis, vasculitis y síndromes oculocutáneos (pigmentación de la piel con opacidades corneanas y del cristalino, y fotosensibilidad).
Este tipo de reacciones dermatológicas aparece con mayor frecuencia en cara, cuello, tronco y extremidades.
A pacientes que desarrollan fotosensibilidad se les debe recomendar protegerse de los rayos solares para evitar quemaduras.
Para los trastornos alérgicos son de utilidad las preparaciones locales con corticoides y los antihistamínicos de tipo HI (terfenadina).
Las dermatitis seborreicas se asocian a los trastornos extrapiramidales.
Oculares
La clorpromazina administrada en dosis alta y crónicamente puede ocasionar, hasta en un 20-30 % de los enfermos, depósitos pigmentarios en la córnea, el cristalino, la conjuntiva, la retina y la piel. Este fenómeno raramente interfiere con la visión.
En cambio, la retinopatía pigmentaria debido al uso de tioridazina, en dosis superiores a los 800 mg/día, produce deterioro de la visión.
Los efectos sobre la acomodación y el empeoramiento del glaucoma de ángulo cerrado son debidos a la acción anticolinérgica.
Los antecedentes de dolor ocular, visión borrosa con halos coloreados, deben decidir la consulta oftalmológica inmediata a fin de iniciar tratamiento específico, si así fuese necesario. En general la visión borrosa se debe a cierto grado de midriasis y cicloplejía, que pueden tratarse con gotas oculares colinomiméticas (pilocarpina al 1 %).
El glaucoma de ángulo abierto presenta menores riesgos que el de ángulo cerrado.
Hematológicas
Los neurolépticos de baja potencia (los dosificables en cientos de mg) pueden producir reacciones tóxicas o alérgicas en la médula ósea con mayor frecuencia que los de alta potencia (los dosificables en décimos de mg). La serie granulocítica es la más atacada, luego de 2-3 meses de tratamiento.
La clorpromazina y la clozapina son las drogas que inducen con más frecuencia estas acciones.
El control clínico sobre las infecciones y el recuento y fórmula leucocitaria son los indicadores más útiles para seguir la evolución de estas reacciones.
Se ha vinculado la clorpromazina a la aparición de anticuerpos antinucleares, al aumento de IgM y a la prolongación del tiempo de tromboplastina asociado o no a esplenomegalia.
Todos estos efectos son reversibles con la discontinuación de la medicación.
Hepáticas
La ictericia colostática es una mezcla de efectos tóxicos y alérgicos.
Se manifiesta al mes de tratamiento, especialmente con los neurolépticos de baja potencia, con fiebre, náusea, dolor abdominal, prurito e ictericia. Las características en el hepatograma son las de una ictericia por obstrucción (aumento de bilirrubina directa y de fosfatasa alcalina) y aparición de ácidos biliares en el plasma.
Las transaminasas pueden estar elevadas pero no llegan nunca a los valores que se encuentran en las hepatitis virales.
La suspensión del antipsicótico hace ceder el cuadro en algunas semanas.
La presencia de trastornos hepáticos o cirrosis no contraindica el uso de neurolépticos, pero se debe tener en cuenta en estos casos el factor de acumulación al encontrarse disminuida la metabolización hepática.
G) Síndrome de abstinencia
Como ya se señaló, la tolerancia ocurre para algunos efectos colaterales como son la sedación, la hipotensión y las acciones anticolinérgicas.
Sin embargo, con discontinuaciones abruptas de antipsicóticos han aparecido en algunos enfermos efectos rebote, recaídas psicóticas y fenómenos colinérgicos (salivación, diarrea, retortijones, insomnio, etc.).
Si estos fenómenos se deben a la hipersensibilización de los receptores, producida por la administración crónica de neurolépticos o a un fenómeno de abstinencia por el aumento o hipersensibilización de los receptores por bloqueo dopamínico, es una hipótesis que tendrá que ser demostrada.
H) Síndrome Inadecuado de Hormona Antidiurética (SIHAD), intoxicación hídrica, hiponatremia
En muchos pacientes psiquiátricos crónicos, y por lo tanto también en los pacientes esquizofrénicos se observan alteraciones de la regulación hídrica. De un 6-17 % de los pacientes psicóticos crónicos y el 70 % de los hospitalizados presentan polidipsia.
Muchos son bebedores compulsivos de agua (20-30 litros o más por día) y secundariamente desarrollan poliuria (síndrome Psicosis-Hiponatremia intermitente-Polidpsia (PIP).
Si la hormona antidiurética (HAD) se libera de manera inadecuada, cuando existe hiponatremia pero con volumen intravascular, normal se genera el síndrome de secreción inadecuada de HAD (SIHAD).
También pueden desarrollar cardiomegalia, fallo congestivo cardíaco, edemas, disfunción urogenital (enuresis, incontinencia, hidronefrosis y fallo renal) y vómitos en chorro.
El 10 % está hiponatrémico y presenta valores alterados de la HAD, con desarrollo franco de intoxicación hídrica que puede llevar al edema cerebral con convulsiones, coma y muerte. Existe hipoosmolaridad plasmática e hiperosmolaridad renal
El tratamiento crónico con neurolépticos convencionales, bloquea el receptor D2, que está asociado a una aumento de la angiotensina 11. De allí que los neurolépticos atípicos tendrían menor propensión a desarrollar el SIHAD. Sin embargo la risperidona bloquea los receptores alfa-2 adrenérgicos y aumenta la HAD en respuesta a la psicosis o al estrés.
El tratamiento de elección, que sería la restricción líquida, no siempre es posible de respetar. Los diuréticos pueden llevar a un círculo vicioso con exacerbación de la polidipsia.
Se puede intentar el tratamiento con beta-bloqueantes (propranolol), con enzimas bloqueadoras de la angiotensina (captopril, 12.5 mg/día; enalapril). La mejoría de la polidipsia y poliuria se acompaña de la del cuadro psicótico, por lo que cabría preguntarse si estos pacientes, que parecen refractarios al tratamiento, no lo son, en parte, debido a los efectos de la intoxicación hídrica sobre el SNC.
El litio, que antagoniza los efectos de la HAD, puede mejorar la hiponatremia, pero puede producir polidipsia y diabetes insípida.
También se ha intentado el bloqueo de los receptores opiáceos, que producen el aumento de la ingesta acuosa, con el bloqueante naltrexona.
Advertencias y precauciones
Las advertencias y precauciones no son contraindicaciones. Para los neurolépticos son las siguientes:
a) Potencian el alcohol, los hipnóticos y los analgésicos.
b) Disminuyen la coordinación motora y el alerta necesario para trabajos de precisión (choferes, actividades manuales de precisión, etc.).
c) Disminuyen el umbral convulsivo (en epilépticos deberá agregarse medicación anticonvulsivante profiláctica).
d) Por su efecto antiemético pueden enmascarar cuadros abdominales agudos, cuadros cerebrales y la intoxicación por litio.
e) No se ha establecido con certeza la ausencia de efectos teratógenos durante el primer trimestre del embarazo.
f) Se deberá prever la posibilidad de que su administración durante el segundo y tercer trimestre del embarazo ocasione ictericia, hiperbilirrubinemia y reacciones extrapiramidales en el recién nacido.
g) Pasan a la leche materna, por lo cual deberá vigilarse la conducta del recién nacido.
h) Por sus efectos anticolinérgicos pueden aumentarla presión intraocular en enfermos con glaucoma y provocar retención urinaria en prostáticos.
i) Pueden agravar la enfermedad de Parkinson.
j) Pueden exacerbar síntomas depresivos.