Volver a ¨Psicofarmacología – Psicodinámica IV (Indice General)¨
6-12. Diferencias entre los IRSS
Se diferencian por sus acciones farmacológicas, metabólicas de interacciones y clínicas. La respuesta terapéutica en pacientes depresivos puede ser desinhibitoria, sedante o mixta.
1) Diferencias farmacodinámicas
Los IRSS tienen potencias diversas, lo que no tiene tina significación clínica relevante en virtud de que a las dosis clínicamente eficaces producen una suficiente inhibición del carrier de 5-HT, como para que sus diferencias sólo se reflejen en el número de mg del comprimido.
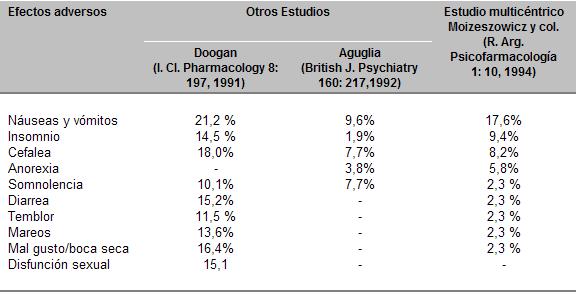
Cuadro 24a. Porcentajes de los efectos adversos en 100 pacientes durante 6 semanas, tratados con sertralina (50-100 mg/día), comparativos con otros estudios
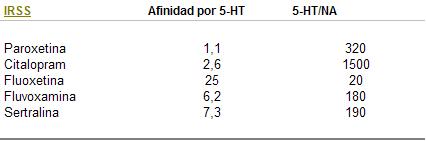
Cuadro 25. Afinidad (N en nM) de los IRSS por el transportador de Serotonina (ST) y selectividad Serotonina/Noradrenalina (NA) (Tomado de Goodwin, 1996)
La paroxetina para algunos y la sertralina para otros son los más potentes (cuadro 25). A su vez, la sertralina es la más potente para la inhibición de la recaptación de dopamina, aun superior a la del bupropión.
La mayor o menor selectividad para 5-HT tampoco se constituye en una diferenciación clínica de relevancia, siempre dentro del espectro de potencias relativas para los carriers de aminas biógenas de estos compuestos. Los estudios in vitro no dan resultados siempre coincidentes. El citalopram es el más selectivo, y el S-citalopram, uno de sus enantiómeros, resulta el IRSS más selectivo que se conoce.
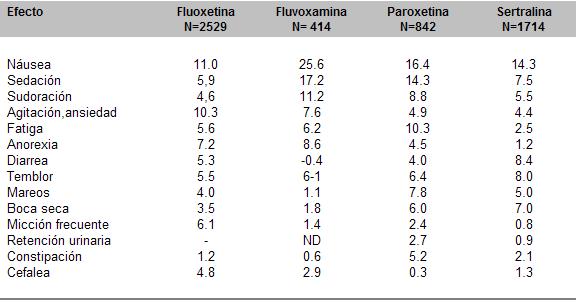
Cuadro 26. Comparación del porcentaje de efectos colaterales de cuatro IRSS (expresados en % restado del placebo) (Tomado de Preskorn, 1995)
La fluoxetina tiene afinidad por el receptor 5HT 2C, lo que puede explicar sus características activantes y ansiogénicas.
La sertralina bloquea el receptor sigma1, que es asociado a la acción antipsicótica y que está en relación con el receptor NMDA.
La paroxetina tiene una leve acción anticolinérgica, con buen efecto sedativo.
2) Diferencias entre los efectos colaterales
La fluoxetina es más activante y tiene una incidencia mayor de cefalea y de micción frecuente.
La fluvoxamina produce náuseas más a menudo, por lo que se recomienda la administración en dos tomas diarias. También tiene una frecuencia mayor de sudoración, sedación y anorexia.
La paroxetina tiene algo de bloqueo colinérgico: retención urinaria y constipación.
La sertralina tiene mayor frecuencia de diarrea. Sin embargo, en el estudio multicéntrico que realizamos, este efecto sólo fue del 2.3%, en los 100 pacientes estudiados con depresión mayor.
Con respecto a la disfunción sexual producida por la sertralina, comparativamente con otros estudios internacionales no hemos encontrado alteraciones en los 100 pacientes. Pese a que la pregunta sobre los efectos adversos fue realizada de manera uniforme («que molestias tuvo Ud. en la última semana»), el tiempo de 6 semanas del estudio tendría que ser suficiente como para poder evidenciarlos, ya que la mayoría de los estudios con otros IRSS abarca igual período de tiempo. Quizás una explicación sería que, para nuestro medio, la compliance con el médico administrador necesita de más tiempo, para tratar el tema de la sexualidad, todavía reprimido para la edad promedio de los pacientes del estudio (46 años).
No se dispone de muchos estudios comparativos de los efectos colaterales de los distintos IRSS, por lo que hay que recurrir a metaanálisis sobre datos que sean cotejables. Las desigualdades tienden a ser de muy poca magnitud (cuadro 26).
3) Diferencias farmacocinéticas
No cabe duda, de que el aspecto de importancia clínica, que más diferencia a los IRSS entre sí, es la farmacocinética (cuadros 27 y 28)
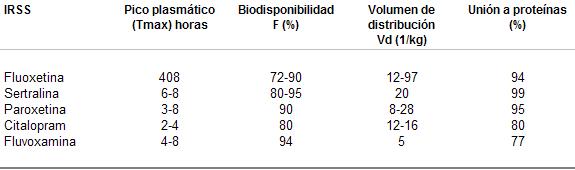
La absorción de los IRSS es lenta y completa, con un pico plasmático(T.. de 3-8 hs., un poco menor para el citalopram (cuadro 27).
La biodisponibilidad (F) es la fracción de la dosis administrada que es absorbida y alcanza la circulación sistémica como droga activa. Depende de la absorción y del pasaje hepático. La sertralina tiene la característica de aumentar la biodisponibilidad cuando se administra con las comidas, cuando se la administra en cápsulas.
El volumen de distribución 1 (Vd), refleja un volumen virtual del cuerpo, que seria necesario, si se supone una concentración uniforme de la droga en todo el organismo. Cuanto más grande, más proporción de la droga está alejada de la circulación general, y por lo tanto más difícil de dialisar en caso de sobredosis.
La diálisis no es útil para remover los tricíclicos. Los IRSS (excepto la fluvoxamina) tienen volúmenes amplios, pero la dificultad de su remoción por diálisis no es importante dada su seguridad en sobredosis.
Todos se encuentran fuertemente unidos a las proteínas plasmáticas, cuando están en la circulación general. El citalopram se vine un poco menos (80 %).
Hay que tener en cuenta, que la fluoxetina y el citalopram, son comercializadas como mezclas racémicas de sus enantiómeros S-y R-, por lo tanto, éstos como sus metabolitos, pueden tener divergencias en sus parámetros farmacocinéticos.
La fuerte unión a proteínas tiene importancia, porque es tina fuente potencial de desplazamiento de drogas de mucha unión, como la warfarina, que circula unida a las proteínas en un 99 %, con las consiguientes interacciones. Sin embargo, los IRSS no tienen mucha afinidad por la alfa-1a, glicoproteína ácida, por lo que no se han reportado interacciones por desplazamiento.
Sólo la fluvoxamina, por razones que no resultan claras, aumenta significativamente la concentración plasmática de la warfarina.
Cuadro 27. Farmacocinética de los IRSS
Cuadro 28. Farmacocinética de los IRSS (Tomado de Preskorn,1997)
4) Diferencias de metabolismo y eliminación: biotransformación
El metabolismo de tina droga puede tener consecuencias sobre sus acciones en el organismo. Si bien su función está destinada a convertir a las sustancias extrañas en metabolitos polares e hidrosolubles, que puedan ser excretados por los riñones, también puede tener otras consecuencias, como cambiarle el perfil farmacodinámico o modificar sus características farmacocinéticas.
Las consecuencias del metabolismo de la fluoxetina tienen importancia clínica, porque su metabolito tiene una vida media de 7-15 días, lo que alimenta enormemente la duración de su acción y el tiempo necesario para alcanzar el estado estacionario.
El estado estacionario o C se obtiene multiplicando el tiempo de vida media (T1/2) por 5. La fluoxetina llega así a 35-75 días de acción.
El concepto de metabolito «activo» puede ser engañoso, ya que tanto puede referirse a la acción antidepresiva como a la acción sobre los citocromos. La fluoxetina se transforma en norfluoxetina, que es una molécula que produce bloqueo de recaptación de 5-HT, con la misma potencia que la droga madre. Puede duplicar la concentración plasmática. Resulta equipotente en cuanto inhibidora del CYP 2D6 y mucho más como inhibidora del 3A3/4.
La sertralina es transformada en N-desmetilsertralina, 10-25 veces menos potente que la droga madre para inhibir la recaptación. Sus niveles plasmáticos llegan a una vez y media los de la sertralina, por lo que su contribución al efecto clínico es pequeña. Es equipotente para la acción sobre los CYP.
La paroxetina se metaboliza principalmente a un intermediario denominado M2 que luego es conjugado y excretado. El producto metabólico es inactivo. Sin embargo, en este caso particular resulta un potente inhibidor del CYP 2D6 in vitro.
El citalopram es transformado en moléculas que no afectarían tanto su actividad clínica como la que tiene sobre los CYP. El más conocido es el desmetilcitalopram. Tanto éste como el didesmetilcitalopram y el citalopramN-óxido tendrían niveles inferiores y actividad inferior a la de la droga madre, tanto en los aspectos dinámicos como quinético.
La fluvoxamina es intensivamente metabolizada, habiéndose encontrado al menos 11 metabolitos en la orina. Se los supone inactivos.
La autoinhibición: describe al fenómeno que se produce cuando hay inhibición de las enzimas que biotransforman una droga, provocada por la misma droga.
La consecuencia es que la vida media aumenta a medida que la concentración lo hace, hasta llegar a la saturación. Esto genera lo que se llama farmacocinética no lineal. En esta situación de saturación el cambio de dosis produce un cambio desproporcionado del nivel plasmático al no producirse un incremento proporcional en la destrucción enzimática. Esta farmacocinética no lineal o «cinética de orden 0» es presentada por la fluoxetina, la paroxetina la fluvoxamina (a dosis muy altas)
El resto de los IRSS tienen una farmacocinética lineal: un cambio de dosis produce una variación proporcional de los niveles plasmáticos, lo que favorece la titulación.
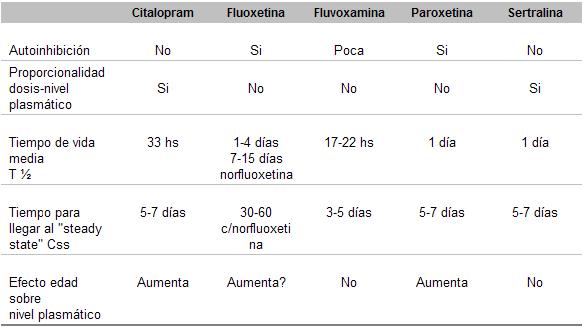
5) Vida media
Cuando es menor de 24 hs., puede ser necesario administrarla en dosis diarias divididas. En los tratamientos de mantenimiento, es más probable la poca adherencia o el olvido repetido de las dosis, lo que aumenta la posibilidad de recaídas [Concentración mínima (Cmin ) por debaio del óptimo)
Cuando es mayor de 24 Irs. puede implicar acumulación gradual, de la droga o sus metabolitos, con aparición de efectos adversos tardíos. Algunos efectos adversos dosis-dependientes de los IRSS (pérdida de la libido, astenia, apatía), también pueden simular síntomas depresivos.
Es necesario cinco T 1/2 para que una droga sea depurada del organismo tras su suspensión. Se debe esperar 2 semanas para pasar de IRSS a IMAO, y cinco semanas para la fluoxetina.
Estos plazos no siempre coinciden: 5 TI 1/2 de la fluvoxamina, son 75 horas. Sus metabolitos son inactivos sobre la recaptación.
La vida media de la fluoxetina, en dosis altas (por ejemplo en el TOC) se prolonga por autoinhibición del metabolismo, y cinco semanas pueden ser insuficientes para la depuración de la droga.
Por otra parte, una T1/2 muy prolongada puede ser ventajosa en pacientes que tienden a olvidar dosis va, que minimiza los olvidos de las mismas (cuadro 28)..
6) Diferencias en la acción sobre los citocromos. Interacciones
Los citocromos P450 o CYP son los encargados de metabolizar a la casi totalidad de las drogas de uso humano. En la última década se aislaron los genes, que codifican para cada uno de los CYP.
Los CYP son varias familias de enzimas, que participan en reacciones oxidativas de esteroidogénesis (de la familia 5 en adelante) o en la oxidación de sustancias ajenas al organismo o xenobióticos (familias 1 a 4). Son alrededor de 30 isoenzimas que se encuentran en todos los tejidos (incluyendo cerebro), pero su mayor concentración es en el hígado y en la pared intestinal.
El primer numero designa a la familia, la letra a la subfamilia, y el último número designa al gen. En algunos casos la homología entre los genes es tan grande que no determina mayores diferencias de acción y se mencionan en forma conjunta (por ej. CYP 3A3/4).
Se conocen las enzimas precisas de la biotransformación de alrededor de un 40 % de las drogas existentes. Al inhibir un (XI? todas las drogas que son transformadas por el mismo aumentarán su nivel plasmático, mientras que lo contrario ocurrirá con su inducción.
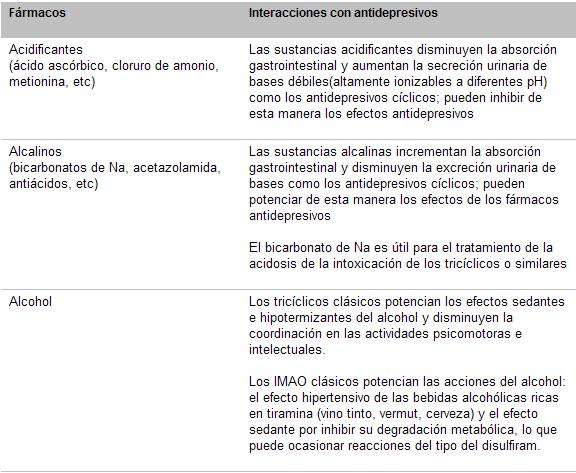
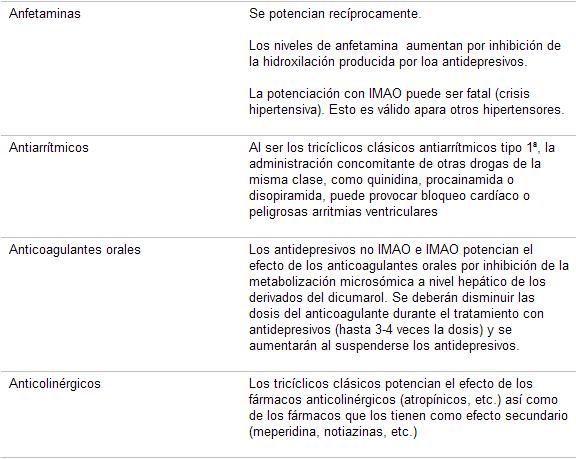
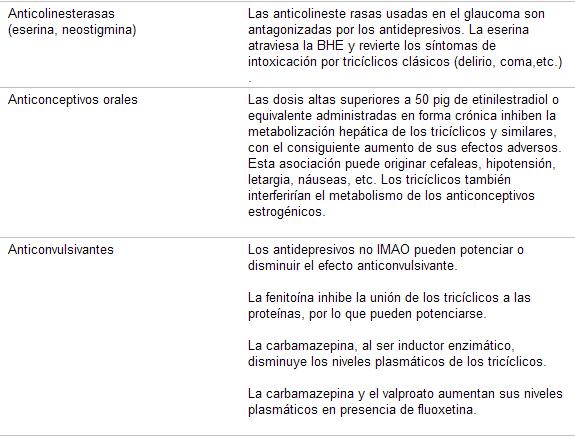
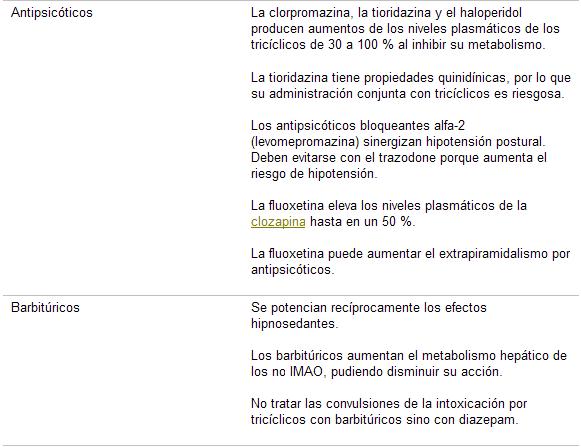
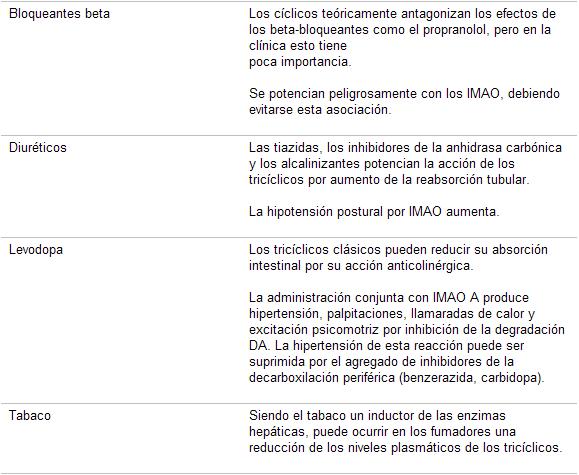
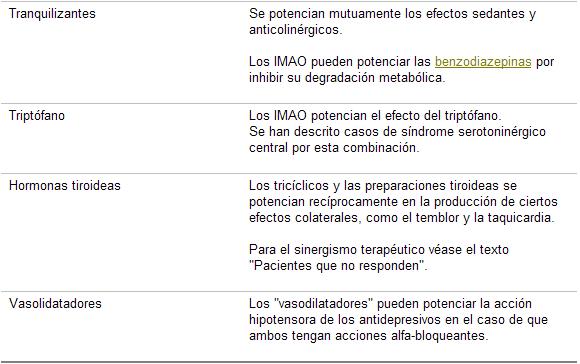
Cuadro 29. Interacciones medicamentosas de los antidepresivos
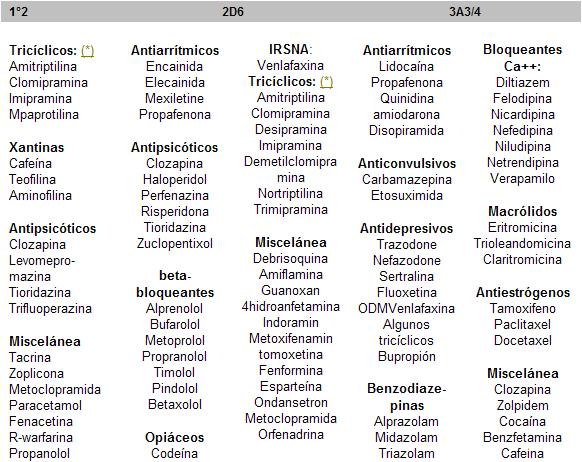
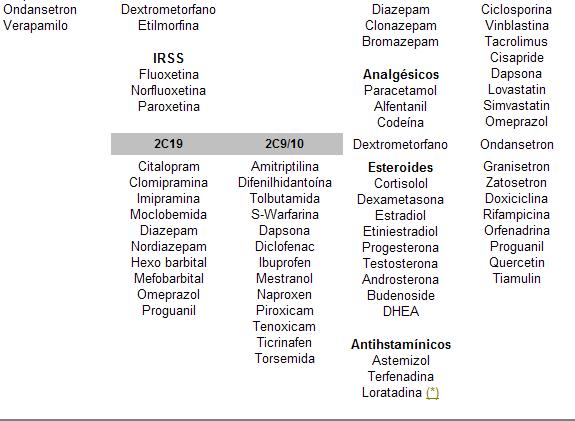
Cuadro 30. Citocromos P450 y sus sustratos
Las interacciones son un motivo de preocupación en el manejo de los pacientes con depresión , ya que son fuente de morbilidad y mortalidad, causa inesperada e inadvertida de fallas al tratamiento, fuente de intolerancias adjudicadas a la «sensibilidad» del paciente. Los deprimidos, sobre todo los añosos, suelen tener prescripciones múltiples por diversos motivos.
Las interacciones mediadas por CYPs, al ser farmacocinéticas, son difíciles de detectar ya que no determinan cambios cualitativos en la respuesta a los fármacos, sino que producen cambios en los niveles plasmáticos que pasan por resistencia o intolerancia (cuadros 29 y 30):
a) CYP 1A2: Este citocromo cataliza la desmetilación de los tricíclicos, aminas terciarias, la clozapina, tacrina, teofilina, cafeína, entre otros. Su inhibición aumenta los niveles plasmáticos de estas drogas. La fluvoxamina es un potente inhibidor de este citocromo, por lo que puede engendrar interacciones significativas.
b) CYP 2D6: Interviene en el metabolismo de los tricíclicos en el paso de amina secundaria a hidroximetabolito. Este paso es muy importante porque su inhibición aumenta enormemente los niveles plasmáticos de los tricíclicos. Es inhibido por la fluoxetina, norfluoxetina y paroxetina. Los reportes de incrementos en las concentraciones plasmáticas de tricíclicos coadministrados con una u otra, en metabolizadores normales, alcanzan desde un 300 a un 640 %, lo que puede inducir una seria toxicidad. La sertralina es el siguiente inhibidor en orden de potencia in vitro, pero sus niveles plasmáticos son más de diez veces inferiores a los de la fluoxetina+ norfluoxetina. Si bien hay reportes aislados de aumentos significativos de niveles de tricíclicos por su interacción, los estudios formales controlados no revelan aumentos mayores de un 40 % a dosis de 50 mg y de 70 % a 200 mg. Debe considerarse una droga de riesgo más bajo a este respecto. La fluvoxamina es el IRSS que menos inhibe este citocromo, pero al inhibir varios otros que actúan en otros pasos metabólicos también eleva los niveles plasmáticos de algunos tricíclicos como las aminas terciarias. El citalopram es un inhibidor débil cuyas interacciones en este sentido deben ser excepcionales
c) El CYP 2D6: interviene también en el metabolismo de los antipsicóticos, antiarrítmicos, opiáceos, beta-bloqueantes.
d) CYP 3A3/4: Es el más abundante, metaboliza a las triazolobenzodiazepinas, así como a los bloqueantes cálcicos y a muchos fármacos más. La terfenadina, el astemizol y el cisapride, al no metabolizarse se convierten en fármacos cardiotóxicos, lo que realza la importancia de conocer las interacciones vía CYP 3A3/4. El ketoconazol y el itraconazol, así como los macrólidos, son inhibidores muy potentes. La carbamazepina es inductora. La fluvoxamina es un inhibidor moderado (alrededor de 100 % de aumento de niveles plasmáticos de sustratos), siendo la fluoxetina más débil (cuadro 29).